Hovedforskel: Fast, flydende, gas og plasma er de fire primære tilstander af materiel, hvor objekter kan findes på Jorden. Fast er en tilstand af materiale, der har en fast form og fast volumen. Væske er en tilstand af materiale, der ikke har nogen fast form, men har et bestemt volumen.

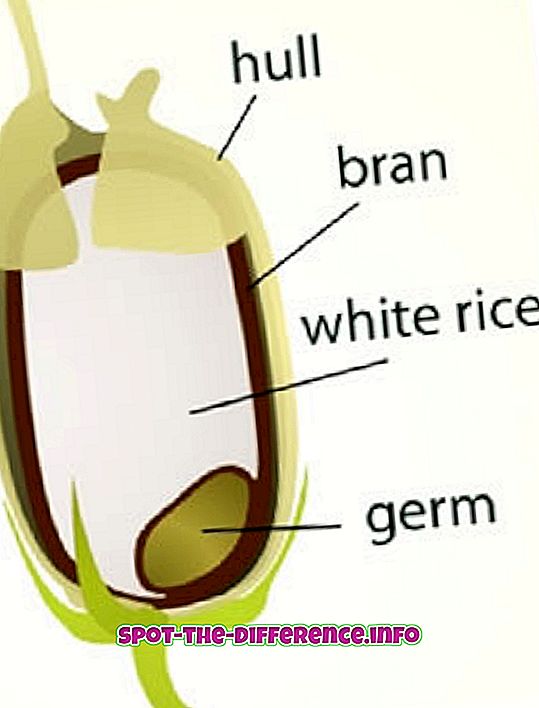
Fast er en tilstand af materiale, der har en fast form og fast volumen. Et fast stof består af små partikler af stof, såsom atomer og molekyler, der holdes sammen af kemiske bindinger. Atomer og molekyler holdes stift på plads, der ikke tillader det faste stof at ændre form eller volumen. Derfor kan et faststof ikke udfylde formen af en beholder som en væske eller fylde alle rum i en beholder som en gas.
Atomer og molekyler i et faststof er tæt bundet til hinanden i enten et almindeligt geometrisk gitter eller uregelmæssigt. Det regelmæssige geometriske gitter er mest almindeligt og kan findes i de fleste faste stoffer, herunder is. Faststoffer med uregelmæssigt bundne atomer er kendt som amorfe faste stoffer. Dette omfatter glas og polystyren.
Når nogle faste stoffer opvarmes, absorberes energien fra varmen af atomerne. Atomerne bliver så ophidsede og begynder at bevæge sig rundt. Obligationerne, der holdt atomet på plads, har tendens til at løsne, så atomerne kan bevæge sig længere væk fra hinanden. I det væsentlige er dette smelteprocessen. Når faststoffet er smeltet grundigt, anses det at være en væske.

Væske er en tilstand af materiale, der ikke har nogen fast form, men har et bestemt volumen. Væske består af små partikler af materiale som atomer og molekyler, der holdes sammen af kemiske bindinger. Væske deler mange af sine egenskaber med de faste og gasformige stater. Som det ligner en gas er det fritflydende og kan tage form af beholderen, den er anbragt i, men i modsætning til en gas kan den ikke fylde alle rum i beholderen. Væskedensiteten er tættere på fast end gas, og begge betegnes som kondenseret materiale. En karakteristisk egenskab af flydende tilstand er overfladespændingen, der resulterer i vædning af genstande, når de dyppes ind i den.
Flydende partikler er bundet fast, men ikke stiv, hvilket giver det evnen til at flyde. De er også i stand til at bevæge sig frit omkring hinanden med begrænset partikelmobilitet. Transformationen af væske til andre stater har at gøre med dets molekyler; som væske opvarmes øges molekylerne i vibrationer og bevægelser, der får dem til at skabe større afstande mellem dem. Efterhånden som afstanden stiger, bliver væsken efterhånden en gas. Under størkning, når væsken afkøles, kommer molekylerne sammen og danner en specifik orden, kendt som krystallisering. Obligationerne mellem dem bliver mere stive og stærkere, og til sidst kommer sammen til at blive en solid. Vand er den mest rigelige væske på jorden og betragtes som en nødvendighed for livets næring.