Hovedforskel: Arrangementet af atomer i et molekyle hjælper med at bestemme dets polaritet. Et molekyle siges at være polært, hvis det har en positiv og en negativ ladning. Et ikke-polært molekyle er et molekyle med mindre ladning.
I kemi refererer polaritet til adskillelsen mellem elektriske ladninger af et molekyle eller dets kemiske gruppe, der har et elektrisk dipol- eller multipolsmoment. Polære molekyler interagerer gennem intermolekylære bindinger og hydrogenbindinger. Molekylær polaritet afhænger af forskellen i elektronegativitet mellem atomer i et molekyle. Polaritet bestemmer også en række fysiske egenskaber som overfladespænding, smeltepunkt og kogepunkt og opløselighed.
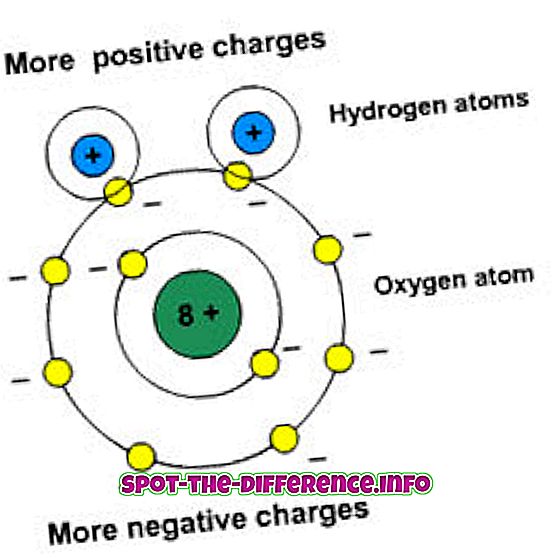
Polaritet betyder adskillelsen af afgifterne. Disse molekyler har et dipolmoment. Dipole-momentet måler polariteten af en obligation. Polære stoffer interagerer med andre polære elementer.

Et ikke-polært molekyle har ikke nok ladning. Ikke-polære molekyler fordeles på en symmetrisk måde og har ikke mange elektriske ladninger på dem. Når to atomer eller to samme atomer har samme elektronbinding mellem dem, trækker atomer elektronparet. Denne træk hjælper dem med at dele elektroner, og denne form for bindingsdeling mellem molekyler er kendt som ikke-polære kovalente bindinger.
Sammenligning mellem polar og ikke-polar:
Polar | Ikke-Polar | |
Definition | Polære stoffer har en positiv og en negativ ladning på atomet. | Ikke-polære stoffer har ikke store afgifter på det vedlagte atom. |
Bevægelse | De har elektrisk dipol bevægelse. | De har ingen dipol bevægelse. |
Opladningsadskillelse | Der er opladning adskillelse. | Der er ingen ladning adskillelse. |
Interaktion | De interagerer med andre polære stoffer. | De interagerer ikke med andre polære stoffer. |
Eksempel | Vand, alkohol og svovl. | Olie. |