Hovedforskel: Den almindeligt accepterede retningslinje er, at organiske forbindelser generelt er forbindelser, der næsten altid indeholder carbon-hydrogenbindinger, mens alt andet ikke klassificeres som uorganiske forbindelser. Der er nogle undtagelser fra denne regel. For det væsentlige afhænger opdelingen af organiske og uorganiske forbindelser af et sæt egenskaber der definerer hvert sæt.

Et molekyle er den mindste mængde af et kemisk stof, der kan eksistere. Som den mindste mængde vand man kan have er et molekyle vand eller H20. Det er sammensat af forskellige atomer sammen; derfor kan det adskilles tilbage i de forskellige atomer.
Forbindelser er opdelt i to hovedkategorier: organiske forbindelser og uorganiske forbindelser. Problemet opstår imidlertid som i løbet af årene har definitionen på hvad der udgør en organisk forbindelse og en uorganisk forbindelse, forskelligt ændret sig væsentligt. Selv nu er der ingen konkret beskrivelse af, hvad der passer til hvilken kategori.
Den almindeligt accepterede retningslinje er, at organiske forbindelser generelt er forbindelser, der næsten altid indeholder carbon-hydrogenbindinger, mens alt andet ikke klassificeres som uorganiske forbindelser. Der er nogle undtagelser fra denne regel. For det væsentlige afhænger opdelingen af organiske og uorganiske forbindelser af et sæt egenskaber der definerer hvert sæt.
Generelle egenskaber ved organiske og uorganiske forbindelser:
Organiske forbindelser | Uorganiske forbindelser |
Mange er gasser, væsker eller faste stoffer | De fleste er faste stoffer |
Normalt indeholder altid carbon, især carbon-hydrogenbindinger | Kan indeholde kulstof. Indeholder metal og andre elementer. Indeholder ikke carbon-hydrogenbindinger. |
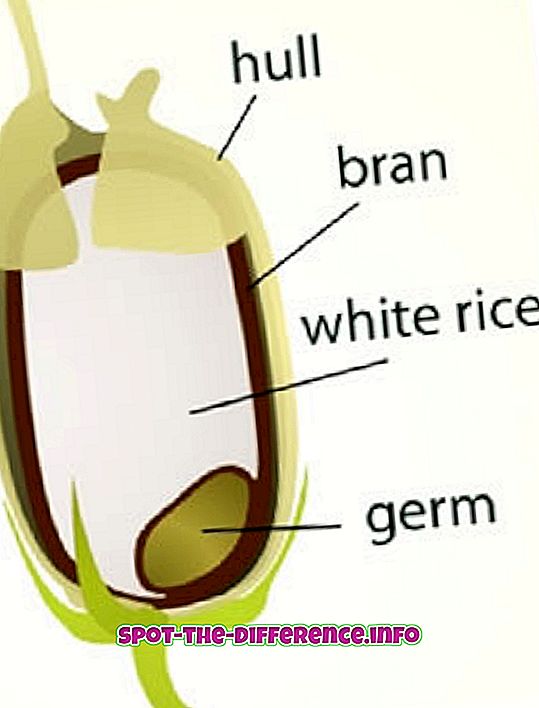
Generelt findes i levende stof, dvs. dyr og planter. | Generelt opnået fra ikke-levende materiale, dvs. mineraler. |
Biologisk i naturen | Mineral i naturen |
Nogle forbindelser er yderst komplekse og har højmolekylære masser. Disse komplekse forbindelser er stabile. | Uorganiske forbindelser er mindre komplekse. Til sammenligning er en kompleks forbindelse generelt mindre stabil. |
Form kovalente bindinger | De fleste former for ionbinding er nogle kovalente bindinger til stede |
Består kun af få elementer, almindeligvis kulstof, hydrogen, oxygen, nitrogen, svovl og fosfor | Består af alle kendte elementer |
Kunne ikke fremstille salte på grund af kovalens af kulstof | Lav salte |
Nedre smeltepunkt og kogepunkt | Højere smeltepunkt og kogepunkt |
Uopløseligt i vand, opløseligt i organiske opløsningsmidler | Letopløseligt i vand, uopløseligt i organiske opløsningsmidler |
Meget brandfarlig og flygtig | Ikke brandfarlig og ikke flygtig |
Dårligere ledere af varme og elektricitet i vandige opløsninger | Bedre ledere af varme og elektricitet i vandige opløsninger |
Langsommere reaktionshastighed | Højere reaktionshastighed |
Producerer mere komplekst sæt produkter under reaktion | Producerer mindre komplekse sæt produkter under reaktion |
Udsæt fænomenet isomerisme | Kun koordineringsforbindelserne viser fænomenet isomerisme |
Klassificeret i mange klasser på grundlag af funktionelle grupper, kendt som homologe serier. Hver klasse er repræsenteret af en generel formel, og medlemmerne viser lignende egenskaber. | Klassificeret som syrer, baser og salte. Ingen homologe serier fundet |
Inkluder nukleinsyrer, fedtstoffer, sukkerarter, proteiner, enzymer og mange brændstoffer. | Inkluder salte, metaller, stoffer fremstillet af enkeltstoffer og andre forbindelser, der ikke indeholder carbon bundet til hydrogen. |
Eksempler: methan, ethan, acetylen, alkoholer, carbontetrachlorid (CCl4), urinstof [CO (NH2) 2] | Eksempler: kuldioxid, svovlsyre, NaCl, diamant (ren kulstof) |