Nøgleforskel: Atommasse er simpelthen massen af en bestemt isotop eller den kombinerede masse af atomets protoner, neutroner og elektroner. Atometallet er antallet af protoner, der findes i en kerne af et element.
Lad os se det, kemi er forvirrende, de forskellige elementer, atomnumre, bindinger, masse, vægt, atomer osv. Alle disse ord begynder at sløre efter en vis tid, at en person ikke længere kan skelne fra hinanden. Godt atommasse og atomnummer er to af sådanne ord, der ofte forveksles og anvendes ombytteligt.
Atommassen er massen af et atom, når den er i ro. Dette skyldes, at når et atom bevæger sig med en meget høj hastighed, har den tendens til at stige i masse. Selvom det ifølge definitionen er atommassen massen af alle protoner, neutroner og elektroner, er elektronerne for små til at gøre nogen væsentlig forskel i atommassen. De fleste af elementerne på det periodiske bord har isotoper og på grund af forskellen i neutrontalet ændres masse af hver isotop også.
Atommassen udtrykkes ved hjælp af atommasseenheder eller amu. En atommasseenhed er lig med 1/12 af massen af Carbon-12. Når massen af et atom er divideret med 1/12 af massen af carbon-12, opnås den relative masse af elementet. Imidlertid er en objekts relative masse faktisk atomvægten af et element, som det beregnes ved at betragte alle isotoperne. Selvom dette ikke bør antages som atommasse af et element.

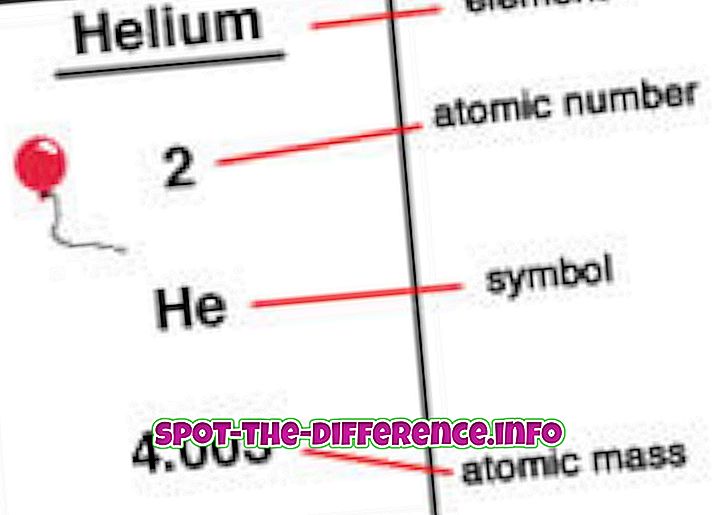
Atometallet er antallet af protoner, der findes i en kerne af et element. Når et atom er neutralt, betyder det, at det har samme antal protoner og elektroner. Atomenummer betegnes med en Z. Da hvert element har et andet antal protoner, bruges dette tal også til at repræsentere et element. Isotoper deler normalt det samme atomnummer, men klassificeres ved hjælp af deres atommasse, for eksempel Carbon-12, Carbon-13.
Elementer placeres i rækkefølge af atomnummer på et periodisk bord. Atomenummeret er opført i elementets venstre øverste hjørne som et superskript. Atomenumre kan hjælpe med at videregive oplysninger om elementet, og mange mennesker kan se atomnummeret og angive hvilket element det er. Det fortæller også, hvor i det periodiske bord det kan placeres, og om det er flydende, gas eller fast. Atomnummer giver også information om kerneladning, oxidationstilstande, bindingsadfærd, ladning af ion etc.